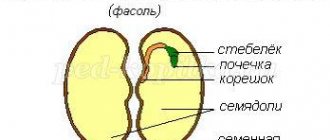
Из чего все состоит. Молекулы
Сейчас тела рассматривают при помощи очень мощных электронных микроскопов. Через них видно, что вещество представлено множеством мельчайших подвижных «кирпичиков». У разных веществ эти «кирпичики» различны. Их называют молекулами. А если представить, что глаза – это «глаза-микроскопы», то мысленно можно увидеть эти маленькие частички.
Молекулы, оказывается, состоят из атомов, а они еще более мелкие частицы. Например, атомы кислорода и водорода, объединившись, образуют знаменитую молекулу воды. Существует шутливая фраза: «Сапоги мои того – пропускают Н2О». Н2О – химическая формула молекулы вода. Н – обозначение водорода, О – кислорода. Индекс 2 в данному случае обозначает число атомов водорода в составе молекулы воды. Молекулы газов водорода и кислорода уже новые. В них по два атома водорода и кислорода (Н2 и О2).
()
Существуют вещества, состоящие только из атомов. Это металлы и инертные газы (например, неон в рекламной иллюминации). Различные комбинации атомов порождают новые вещества, существующие в природе.
Люди очень давно предполагали, что вещества составлены из молекул и атомов. Еще в пятом веке до нашей эры ученый Древней Греции Демокрит высказал такую гипотезу. В России учение о молекулярном строении вещества развил М.В. Ломоносов в восемнадцатом веке.
Как же оценить размеры загадочных маленьких частиц?
Следуя правилу измерения, их нужно с чем-то сравнить. Интересен такой мысленный эксперимент: семиклассник и молекула. Если молекулу увеличить в несколько раз так, чтобы она стала размером с семиклассника, но и его увеличить во столько же раз, то семиклассник может достать до Солнца. Наука, конечно, не пользуется такими сравнениями. Современные приборы — микроскопы позволяют найти размеры атомов и молекул довольно точно. Существует возможность подсчитать и количество маленьких частиц в любом теле.
Легко догадаться, что число молекул вещества огромно. И опять интересное сравнение: если бы людей на планете Земля было столько, сколько молекул в одном кубическом сантиметре воздуха, то на одном квадратном километре Земли могли бы уместиться пять тысяч человек.
Итак, вещество состоит из молекул, а молекулы из атомов;
- разные вещества по структуре имеют разные молекулы (комбинации атомов);
- молекулы микроскопически малы, а в теле их огромное количество.
Строение вещества. Молекулы
Строение вещества
Познать сущее нельзя извне, можно только изнутри
Николай Бердяев
Данная тема посвящена строению вещества. Еще в древности люди высказывали предположения о том, что все вещества состоят из очень маленьких частичек
. Однако лишь в восемнадцатом веке эти предположения сложились в более или менее стройную теорию. Представления о строении вещества помогли людям не только понять и объяснить те или иные физические явления, но и влиять на происхождение явлений, предсказывать поведение различных веществ при изменении внешних условий. Более того, люди научились сами получать вещества с заданными свойствами.
Некоторые явления можно легко предсказать, опираясь на свой повседневный опыт. Например, если сжать руками воздушный шарик, то он изменит свой объем и форму.
Если развязать шарик, то из него выйдет воздух. Если капнуть каплю краски в воду, то вода окрасится. Если нагреть лед, то он растает и превратится в воду.
Рассмотрим несколько целенаправленных опытов, которые дадут некоторые сведения о строении вещества. Возьмем самый обычный листочек с дерева. Можно ли его разделить? Конечно, легко можно его разорвать. Полученные кусочки можно разорвать ещё и ещё. Если растереть маленький кусочек листика пальцами, то можно увидеть, мелкие частички, оставшиеся у вас на пальцах. Можно провести аналогичный опыт с водой. Если взять бутылку, в которой находится некоторое количество воды.
Легко можно перелить часть воды в другую ёмкость, а из этой ёмкости – в еще одну, и так далее. Подобные опыты говорят нам, что самые различные вещества состоят из частиц.
Сжимая шарик, можно добиться уменьшения его объёма. При этом следует заметить, что количество частиц воздуха внутри шарика не изменилось
. Следовательно,
уменьшилось расстояние между частицами
.
Аналогично, можно растянуть резиновый шнурок, тем самым увеличив его объём
. Опять же,
количество частиц от этого не меняется.
Следовательно, увеличивается расстояние между частицами. Таким образом,
вещество состоит из частиц, и между этими частицами есть определенные промежутки.Но только ли механическими усилиями можно уменьшить или увеличить эти промежутки?
Оказывается, что
нет
. Можно провести следующий опыт: проденем шарик, подвешенный на цепочке через кольцо.
Нагреем этот шарик и попытаемся вытащить его обратно. После нагревания шарик в кольцо не пролезает. Это говорит о том, что при нагревании тела расширяются, то есть, увеличивается их объём.
Если подождать, пока шарик остынет, то он снова сможет пройти через кольцо. Значит,
при охлаждении, объем тела уменьшается.То же самое будет происходить и с жидкостью.
Наполним сосуд водой до краев и закупорим его пробкой. В пробку проденем маленькую стеклянную трубку.
При нагревании вода частично заполнит трубку, а, значит, объём воды тоже увеличивается при нагревании.
Это хорошо подтверждается и другим бытовым опытом:
если в сосуд с горячей водой опустить термометр, то столбик ртути поползет вверх.
То есть,
при нагревании ртути, промежутки между её частицами увеличиваются, что приводит к увеличению объёма.
Таким образом, когда частицы тела отдаляются друг от друга, объём тела увеличивается
. И наоборот,
когда частицы тела сближаются друг с другом, объём тела уменьшается.
Может возникнуть вопрос:
о каких частицах идет речь, если все тела являются сплошными и их можно перемещать целиком, не волнуясь о том, что эти частицы рассыплются?!
Более детальное объяснения этих вопросов, будет раскрыто при дальнейшем изучении физики. Тем не менее, можно провести довольно простой опыт, подтверждающий, что вещество состоит из частиц. Возьмем три стакана с водой и окрасим воду в одном из них.
Перенесем часть окрашенной воды в другой стакан. Видно, что вода в этом стакане тоже окрасилась, но цвет менее насыщенный. Если затем перенести часть воды из второго стакана в третий, то вода в нем тоже окрасится, но совсем немного. Этот опыт подтверждает, что вещество состоит из частиц.
Все меньшая насыщенность цвета в стаканах объясняется присутствием меньшего количества частиц краски.
И это, конечно, лишь один из множества опытов, подтверждающих то, что вещества состоят из мельчайших частичек.
Такие частички были названы молекулами
. Молекула в переводе с латинского языка означает «
маленькая масса
».
Размеры молекул настолько малы, что человеческий глаз просто не в состоянии увидеть отдельные молекулы.
Чтобы представить, насколько малы молекулы, приведем несколько примеров. Например, в яблоке содержится примерно столько же молекул, сколько яблок можно было бы уложить внутри нашей планеты – Земли. Ещё один пример: в одной капле воды содержится примерно столько же молекул, сколько капель содержится в Черном море. В очень малом объёме воздуха – в одном кубическом миллиметре содержится 27×1015, то есть миллионы миллиардов молекул. Конечно, столь малые частицы мы не в состоянии увидеть без специальных приборов.
Один из таких приборов называется электронным микроскопом:с его помощью, мы можем увидеть молекулы и получить их изображения.
Например, на рисунке представлен один из видов частичек крови – эритроциты, а также витамин C.
На сегодняшний день ученые изучили множество различных молекул и с уверенностью могут сказать, что молекулы разных веществ отличаются друг от друга, но молекулы одинаковых веществ абсолютно одинаковы.
Таким образом, из молекул воды может состоять только вода и ничего больше. Однако, даже
молекулы не являются наиболее мелкими частицами
.
Они состоят из атомов
(
атом в переводе с греческого означает «неделимый»
). При дальнейшем изучении физики будет показано, что и атом имеет внутреннее строение. Молекулы принято изображать схематически: вот, например, схематическое изображение молекулы воды: она состоит из двух атомов водорода и одного атома кислорода.
Каждое вещество имеет своё обозначение.
Например,
водород обозначается латинской буквойH, а кислород – буквой О
. Таким образом, молекула воды имеет химическую формулу
H2O– эта формула показывает, что в молекуле два атома водорода и только один атом кислорода.
Если молекулы состоят из атомов, почему же, молекулы считаются наименьшими частицами данного вещества?
Дело здесь вот в чем: молекулы образуют вещество таким, каким мы его видим, осязаем, ощущаем и так далее.
Основные выводы:
– Все тела состоят из частиц
.
– Между этими частицами есть промежутки.
– Размеры
этих частиц
очень и очень малы
.
– Наименьшие частицы
данного вещества называются
молекулами
.
– Молекулы
состоят из
атомов
.
– При нагревании
тела
расширяются
, а при
охлаждении
–
сжимаются
.
Движение молекул
Будет ли чай в стакане сладким, если сахар в нем не перемешивать? Да, конечно. Но через определенное время, за которое молекулы сахара со дна стакана поднимутся в верхние слои жидкости. Значит, молекулы движутся. Как они движутся и где?
Простой опыт:
Если в полстакана крупы засыпать без перемешивания полстакана гороха, получится целый стакан. Крупинки и горошинки небольшие, но не могут «протиснуться» в пустые промежутки.
А если в мензурку налить по одинаковому количеству воды и спирта? Увеличения смеси в два раза, как в первом случае, не получится. Почему? Молекулы воды и спирта совершенно разные. Между молекулами воды расстояния больше, чем между молекулами спирта. Вот эти промежутки частично и заполняются, уменьшая объем смеси.
Таким же образом молекулы сахара «разбегаются» по всему объему, делая чай сладким.
(Источники и )
Проникновение молекул одного вещества в промежутки между молекулами другого называется диффузией.
В газах диффузия – тоже довольно частый процесс. Проходя мимо кондитерской фабрики, люди наслаждаются запахом карамели, зефира, шоколада, входя в парикмахерскую, ощущают аромат духов, одеколона, туалетной воды. Человека постоянно сопровождают запахи. Они несут важную информацию о веществе, благодаря диффузии. В газах она протекает быстрее, чем в жидкостях, и вот почему. Межмолекулярные расстояния в газах больше, чем в жидкостях, отсюда возможности для движения больше.
А возможна ли диффузия в твердых телах? Нужно учитывать, что твердое тело держит форму без изменения, благодаря расстояниям, близким к размерам самих молекул или даже меньше их. Могут ли туда проникнуть «чужие» молекулы? Оказывается, диффузия в твердых телах тоже возможна, но при условии, что они находятся в очень тесном контакте друг с другом. Процесс длится очень медленно, и время измеряется годами. Известен опыт с двумя отшлифованными телами из золота и свинца. Их плотно прижали друг к другу и оставили под наблюдением. Диффузия произошла. Всего на 1 мм за пять лет.
()
Движение молекул и промежутки между ними объясняют диффузию. Гипотезу об этом впервые высказал греческий ученый Эпикур в III веке до н.э.
Опытным путем доказал это в 1827 г. Броун, знаменитый английский ботаник. Он рассмотрел через микроскоп споры растения плаун, находящегося в воде, и заметил, что эти маленькие частички постоянно двигаются в разных направлениях. Безостановочное, беспорядочное движение продолжалось и днем, и ночью, в любое время года. Почему же двигались споры растения? А двигались они потому, что их толкали и заставляли двигаться невидимые в простой микроскоп молекулы воды.
Молекулы движутся постоянно, сближаются друг с другом и, отталкиваясь, приобретают новое направление движения. Их много в веществе, и встречи, изменяющие направление, происходят очень часто. Суммарный удар нескольких молекул приводит в движение небольшие частицы, попавшие в воду. Движение этих частиц назвали броуновским движением, а сами частицы – броуновскими.
()
Итак, следует запомнить:
- Между молекулами существуют промежутки
- Молекулы движутся хаотично и постоянно
- Явление проникновения молекул одного вещества в промежутки между молекулами другого называется диффузией.
Вариант 1
1. Мельчайшие частицы, из которых состоят различные вещества, называются …
А. атомами Б. молекулами
2. Все молекулы одного и того же вещества …
А. не отличаются друг от друга Б. отличаются друг от друга
3. При охлаждении объем тела …
А. уменьшается Б. увеличивается
4. Как зависит процесс диффузии от температуры?
А. процесс диффузии замедляется с ростом температуры Б. процесс диффузии ускоряется с ростом температуры В. процесс диффузии не зависит от изменения температуры
5. На расстояниях, сравнимых с размерами самих молекул (атомов) …
А. заметнее проявляются силы притяжения между молекулами, а при дальнейшем сближении — силы отталкивания Б. заметнее проявляются силы отталкивания между молекулами, а при дальнейшем сближении — силы притяжения
6. Какие из указанных свойств принадлежат газам?
А. имеют собственную форму Б. сохраняют объем В. не имеют собственной формы и постоянного объема
7. Как расположены молекулы газа?
А. двигаясь беспорядочно во всех направлениях, почти не притягиваются друг к другу Б. не расходятся на большие расстояния В. расположены в определенном порядке
8. В каком состоянии может находиться ртуть?
А. только в жидком Б. в жидком, твердом и газообразном В. только в твердом
9. Можно ли открытый сосуд заполнить газом на 40% его вместимости?
А. да, можно Б. нет, нельзя В. определенного ответа дать нельзя
10. Вода замерзла и превратилась в лед. Изменились ли при этом сами молекулы воды?
А. нет, не изменились Б. да, изменились В. определенного ответа дать нельзя
Температура
Благодаря комбинациям атомов у разных веществ молекулы неодинаковы. А если рассмотреть одно вещество, но в разных ситуациях, например, воду из водопроводного крана, в кружке чая или весеннем ручейке. Во всех трех случаях молекулы одни и те же, но ведут они себя по-разному. В горячем чае молекулы движутся наиболее быстро. В холодном ручейке гораздо медленнее. А в воде из крана молекулы движутся медленнее, чем в горячем чае, но быстрее, чем в ручейке.
(Источники и )
Конечно, речь здесь идет о таких скоростях, с которыми человек не может передвигаться. Человек может идти со скоростью 4 – 7 км/ч. Скорость молекулы воды при комнатной температуре в среднем 590 м/с = 2124 км/ч (в кипящей воде — ≈ 2340км/ч) Это надо понимать, когда говорят, что одни молекулы движутся быстро, а другие медленно.
Когда говорят «холодно», «тепло», «горячо», то сравнивают температуру. Определяется температура любого тела тем, как движутся молекулы этого тела: быстро или медленно. Температура тем выше, чем быстрее передвигаются молекулы. Если же молекулы начинают двигаться медленнее, то и температура тела понижается.
Окружающая нас природа зависит от температуры. С понижением ее приходит осень, а потом зима. С ростом температуры зима уступает место весне, а весна – лету.
Свойства вещества также зависят от температуры. Например, мягкая резина на холоде становится твердой, а твердый лед превращается в жидкость, если его занести в теплую комнату.
Температура характеризует свойства живой и неживой природы. Значит, о ней многое нужно знать. Главное надо запомнить это: скорость движения молекул, образующих вещество, определяет его температуру.
Чтобы измерить температуру, используют приборы – термометры. Термометры бывают по назначению:
- лабораторные;
- медицинские;
- уличные;
- комнатные;
- технические.
по конструкции:
- жидкостные;
- газовые;
- механические;
- электрические;
- оптические.
Температура измеряется в градусах. В 1742 году шведский геолог, метеоролог и астроном Андрес Цельсий придумал шкалу, в основе которой лежат отсчетные точки: температура таяния льда (0 градусов) и температура кипения воды (100 градусов).
()
В 1848 году Уильям Томсон (лорд Кельвин) ввел понятие абсолютного нуля температуры (-273 градуса, минимальная возможная температура во Вселенной). При этом, температура таяния льда уже 273 градуса и соответственно кипения воды 373 градуса.
()
В 1724 году польско-немецкий ученый Даниель Габриель Фаренгейт создал свою шкалу, которая использовала в англоязычных странах. Сейчас она используется только в США.
()
На всех трех шкалах используются две основные точки – температуры перехода выбранного вещества из одного состояния в другое.
На шкалах Цельсия и Кельвина этим веществом выбраны вода, а две точки – это температура таяния льда и кипения воды. Промежуток между этими температурами разделен на 100 частей, таким образом получен 1 градус.
Цельсий выбрал за 0о температуру плавления льда. Кельвин обозначил нулем минимальную возможную температуру (когда движение молекул прекращено). Тогда по Цельсию лед плавится при 0о С (по Кельвину при — 273о К), вода кипит при 100о С, а по Кельвину при 373о К, так как нуль Кельвина ниже нуля Цельсия на 273о. При переходе от градусов Цельсия к градусам Кельвина нужно прибавлять 273 градуса.
Фаренгейт основными точками назвал температуру, близкую к температуре застывания ртути и нормальную температуру человеческого тела. В результате температура таяния льда Фаренгейта выше примерно на 32 градуса температуры Цельсия.
Пример перехода от одной шкалы к другой:
нормальная комнатная температура
- по шкале Цельсия – 20о С;
- по шкале Кельвина – оС + 273о = 20о С + 273о = 293о К;
- по шкале Фаренгейта – о С ∙ 9/5 + 32о = 20о С ∙ 9/5 + 32о = 68о F.
Наиболее рациональной и простой в использовании считается шкала Цельсия.
(Подробно температура изучается в старших классах в разделах «Тепловые явления» и «Термодинамика»).
Молекулы в любых условиях движутся постоянно и хаотично. Движение влияет на температуру, поэтому называется оно тепловым. Тепловое движение передается и броуновским частицам. Определение этого явления: движение частиц твердого вещества, попавших в жидкость, под действием теплового движения молекул жидкости называется броуновским движением.
Итак:
- Движение молекул определяет температуру тела
- Температура измеряется термометром по шкалам Цельсия, Кельвина, Фаренгейта
- Температура – физическая характеристика тела
Конспект урока по физике в 7 классе по теме: «Строение вещества.Молекулы».
Урок физики по теме «Строение вещества. Молекулы». 7-й класс
Цели:
· Образовательная: познакомить учащихся со строением вещества. Дать представление о размерах молекул.
· Развивающая: развивать логическое и образное мышление.
· Воспитывающая: воспитывать в процессе обучения трудолюбие, чувство ответственности и дисциплины
Задачи урока:
· ввести понятие « атом» и «молекула» как модели строения вещества;
· выделить экспериментальное исследование в процессе познания;
· подчеркнуть значение моделирования вещества в познаваемости явлений окружающего мира;
· формирование умений делать выводы из наблюдений;
· формировать желание учащихся в познании явлений природы
Оборудование: штатив с кольцом, медный или латунный шарик, который проходит через кольцо штатива, колба, стеклянная трубочка, спиртовка, марганцовка.
ХОД УРОКА
1. Организационный момент
Проверка отсутствующих, внешнее состояние кабинета, рабочих мест, наличие дежурных.
2. Актуализация знаний
1) Что значит измерить какую-либо величину?
Ответ: измерить какую-либо величину – это значит сравнить её с однородной величиной, принятой за единицу.
2) Как определяется цена деления шкалы измерительного прибора?
Ответ: для того чтобы определить цену деления шкалы, необходимо:
– найти два ближайших штриха шкалы, возле которых написаны значения величины; – вычесть из большего значения меньшее и полученное число разделить на число делений между ними.
3) Почему каждому нужно знать физику? Ответ:
1) физика объясняет причины разных явлений, 2) позволяет создавать новую, всё более совершенную технику; 3) даёт знания о самых общих законах природы, играющих большую роль в жизни каждого человека.
3. Изучение нового материала»Строение вещества. Молекулы»
Учитель: Ребята, мы с вами познакомились с понятием вещество. Кто помнитчто называется веществом?
Ученик: Всёто из чего состоят физические тела называется веществом. Вещество – это вид материи, а материя – это всё то, что существует во Вселенной независимо от нас.
Учитель: Правильно! Сегодня мы с вами узнаем из чего же состоит вещество. Всёокружающее человека – вода, воздух, горы, деревья – обладают своимисвойствами. Ещё в глубокой древности, 2500 лет назад, некоторые учёные высказали предположение о строение вещества.
Греческий учёный Демокрит (460-370 до н.э.) считал, что все вещества состоят из мельчайших частичек.
В научную теорию эта идея превратилась только в XVIII в. и получила дальнейшее развитие в XIX в.
Возникновение представлений о строении вещества позволило объяснить многие явления, предсказать, как они будут протекать в тех или иных условиях. Появилась возможность влиять на прохождение явлений. Многие опыты подтверждают представления о строении вещества. Рассмотрим некоторые из них. Попытаемся сжать теннисный мячик. При этом объём воздуха, который наполнял мяч,уменьшится. Можно уменьшить объём надувного шарика, и кусочка воска, если приложить некоторое усилие. Объём тела также меняется при нагревании. Проделаем опыт.
Демонстрация опыта: возьмём медный или латунный шарик, который проходит через кольцо штатива. Давайте нагреем шарик и посмотрим что с ним произойдёт. Если шарик нагреть, то, он расширится и уже сквозь кольцо не пройдёт . Через некоторое время шарик, остыв, уменьшится в объёме, а кольцо, нагревшись от шарика, расширится, и шарик вновь пройдёт через кольцо.
Второй опыт: Колбу, наполненную доверху водой плотно закроем пробкой. Сквозь пробку пропустим стеклянную трубочку. Вода частично заполнит трубку. Отметим уровень жидкости в трубке. Нагревая колбу, мы заметим, что через некоторое время уровень воды в трубке поднимается.
Рисунок №2
Следовательно, при нагревании объём тела увеличивается, а при охлаждении уменьшается. А сейчас поделимся на группы и каждая группа будет проводить опыты самостоятельно и в конце сделает экспериментальный вывод.
4. Групповая работа
Карточка № 1.
Приборы и материалы: мел, пузырек с кристаллами марганцево-кислого калия, 3 стакана с чистой водой, стеклянная палочка.
Ход работы
1. Проведите пальцем по поверхности мела. Что вы наблюдаете? Что вы можете сказать о размерах частиц, из которых состоит мел? 2. Бросьте в стакан с чистой водой несколько крупинок марганцовки. Размешайте раствор палочкой и перелейте несколько капель во второй стакан, затем повторите эту процедуру еще раз. Сравните цвет раствора во всех трех стаканах. 3. Ответьте на вопросы:
Рисунок №3
– Сохранилось ли основное свойство вещества – цвет? – Можете ли вы сделать предположение о том, сколько частичек марганцовки осталось в третьем стакане? А сколько их тогда было в первом стакане? – Вспомнив размеры кристалликов, брошенных вами в воду, можете ли вы сказать, что- либо о размерах мельчайших частиц вещества?
5. Обсуждение групповой работы и выдвижение гипотезы о строении вещества
· Объём тела при нагревании увеличивается, а при охлаждении уменьшается.
· Все вещества состоят из отдельных частичек, между которыми имеются промежутки.
· Если частицы удаляются друг от друга, то объём тела увеличивается.
· Когда частицы сближаются, объём тела уменьшается.
· Если все тела состоят из мельчайших частиц, почему они кажутся нам сплошными?
Молекула вещества – мельчайшая частица данного вещества
1. При помощи электронного микроскопа удалось сфотографировать расположение молекул белка. 2. Молекулы разных веществ отличаются друг от друга, а молекулы одного и того же вещества одинаковы.
Рисунок №4
Молекулы состоят из маленьких частиц – атомов
Рисунок №5
1. Атомы – частицы из которых состоят молекулы.
2. Атомы принято обозначать специальными символами.
3. О – атом кислорода
4. Н – атом водорода
5. С – атом углерода
6. Закрепление
Когда мы выдвинули гипотезу, надо проверить её, попытаться объяснить с её помощью различные факты. Давайте решим несколько задач. 1. Рука золотой статуи в древнегреческом храме, которую целовали прихожане, за десятки лет заметно похудела. Священники в панике. Кто то украл золото! Или это чудо, знамение? Объясните на основе гипотезы Демокрита о существовании мельчайших частиц вещества, что же произошло. 2. Износ обуви, углубления в ступенях древних лестниц, протирание локтей пиджаков, брюк… Не наводят ли эти будничные явления на глубокие научные размышления? На какие? 3. Вы делаете уроки. Из кухни доносится аппетитный запах жаренной картошки…Как это могло произойти согласно гипотезы Демокрита? Не доказывает ли распространение запахов существование промежутков между молекулами?
7. Домашнее задание: параграф 6, 7 (составить план ответа), упр. 2.
8. Итог
– Что нового вы узнали из этого урока? Что всё нас окружающее состоит из молекул и атомов. Как интересна наука физика, которая знакомит нас с такими наблюдениями, опытами и гипотезами, т.е. догадками о том, как протекает явление. И так греческий ученныйДемокрит предположил, что все вещества состоят из мельчайших частичек, а развитие эта гипотеза получила в ХIXвеке.
Взаимодействие молекул
Все тела состоят из движущихся молекул. Между ними есть промежутки. Встает вопрос: почему тела не рассыпаются на молекулы или мелкие крошки? Наоборот, ломая деревянную палку, надо сильно потрудиться.
()
Молекулы крепко удерживаются вместе. А если попытаться соединить две части сломанной палки, она целой не станет. Значит, между молекулами есть постоянная связь (взаимодействие).
Тела не распадаются на отдельные частички, благодаря притяжению молекул и атомов. С другой стороны, если бы существовало только межмолекулярное притяжение, то не было бы среди молекул промежутков, а они есть. Значит, должно быть и отталкивание. Но оно начинает проявляться при условии, когда молекулы сближаются на расстояния, меньшие размеров самих молекул. Чем ближе сдвигаются молекулы, тем сильнее они отталкиваются.
В случае со сломанной палкой края обломков разрушились, и человек не может просто так, одними руками, соединить их так близко, чтобы молекулы начали взаимодействовать. Поэтому результат опыта будет нулевым.
А теперь другой эксперимент. Нужно разъединить два стеклянных листа, лежащих друг на друге.
()
Сделать это не просто. Почему? Нетрудно догадаться. Молекулы обоих листов достаточно близки, так как листы очень гладкие. Наступает взаимодействие (притяжение молекул).
Влажный бумажный лист гораздо труднее поднять, чем сухой с полированной крышки стола. В жидкости молекулы легче сдвинуть на расстояния, когда начинает возникать притяжение. Если две отдельные капельки воды соединить, то они сольются в одну.
Наблюдается взаимное притяжение жидкости к твердому телу. Оно называется смачиванием. Например, вода смачивает многие ткани, дерево, бумагу, но к пластилину, воску, жирным поверхностям не притягивается. Этот процесс называется несмачиванием. Смачивание и несмачивание встречается в быту, технике, живой и неживой природе.
В каких случаях будет наблюдаться смачивание, а в каких несмачивание?
Итак:
- Между молекулами действует взаимное притяжение и отталкивание
- Величина притяжения и отталкивания определяется расстоянием между молекулами
- Взаимодействовать друг с другом могут молекулы и атомы различных веществ
Основы
Три опорных факта составили первоначальные сведения о строении вещества. Приведем их:
- Всякие тела (газы, жидкости, кристаллы, аморфные тела) состоят из молекул и атомов. Позднее Фарадеем было введено понятие ионов – положительно (катионы) или отрицательно (анионы) заряженных частиц, которые могут состоять из одного или более атомов.
- Частицы, из которых состоят тела, обладают кинетической энергией и пребывают в состоянии постоянного движения (для газов и жидкостей – хаотическое движение, для твердых тел – малые колебания).
- Частицы взаимодействуют друг с другом, притягивают друг друга и отталкивают, испытывают упругие соударения. Позднее все взаимодействия рассматривали как электромагнитные.
Рис. 1. Броуновское движение.
К этим идеям пришли не умозрительно, а через опыт. Броуновское движение взвешенных частиц под воздействием ударов молекул, диффузия газов и жидкостей, изменение объема веществ в результате нагревания или остывания и так далее. Изначально атомы представляли некими мельчайшими частицами, «шариками». Вопрос о размерах и весе был снят еще в середине 19-го века, когда обнаружили электрон – частицу, которая была легче водорода в 1840 раз. Но об их структуре представления так или иначе не было. Несмотря на это Менделееву удалось создать периодическую систему элементов, уточнить атомные массы многих веществ (урана, бериллия и других).
Большой вклад в развитие теории внесли Фарадей (объяснил электролиз) и Максвелл (оценил средний пробег молекул газа, заложил основы статистической механики).
Об атомах знали также, что они могут объединяться между собой. Два и более атомов, объединенных в общую структуру, и есть молекула. Если атомы разные, то вещество называли сложными, если одинаковые – простым.
Рис. 2. Молекулы сложных веществ.
На основе этих представлений были объяснены различия в строении между твердыми, жидкими и газообразными телами. Твердые тела описали как упорядоченные плотные пачки колеблющихся атомов, соединенных жесткой связью (электростатическое взаимодействие), а жидкости и газы – как облако беспорядочно движущихся частиц (но в газах расстояние между ними много больше их собственных размеров).
Рис. 3. Строение твердых тел.
Три агрегатных состояния
Какое вещество на Земле самое привычное и распространенное? Конечно, вода. Вода встречается повсюду, причем в разном виде (лед или снег, жидкость, пар). Это агрегатные состояния воды.
(Источники , и )
Абсолютно все вещества меняют внешний вид и свойства. Происходит это при определенной для каждого вещества температуре. Кислород, если его охладить до – 183о С бывает голубой жидкостью, а железо кипит при 2750о С. Непривычно, но это так.